肝细胞体外培养系统,简称生物人工肝,是指人工培养的肝细胞作为基本单元的体外生物反应系统。肝细胞体外培养系统与人体血液循环通路连接,为急性肝衰竭等肝病患者提供体外肝脏功能支持。基于此,中科院力学所技术团队发展了以下两种相关的关键技术:
1)体外三维肝血窦模型:
鉴于成熟肝细胞不能体外增殖,离体肝细胞功能体外维持时间的长短是限制生物型人工肝应用的关键因素,而肝血窦作为肝脏的主要微循环网络,是肝细胞在体生存的主要场所,具有复杂的结构组成及力学、物理微环境。体外三维肝血窦模型是以模拟肝细胞的生理微环境为目标,深化肝血窦微组织结构-功能关系,优化肝细胞体外生长环境。
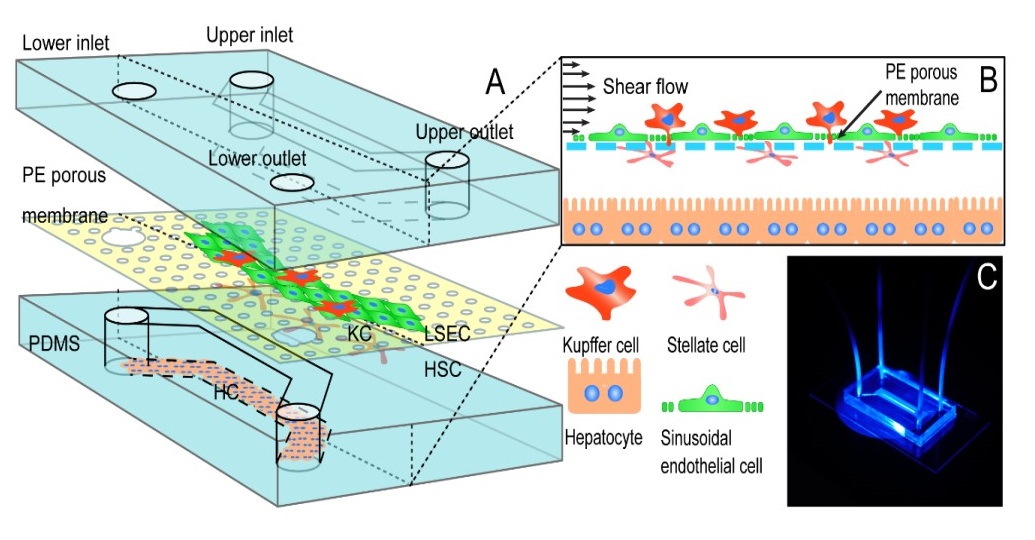
体外三维肝血窦模型模式图
我们研发了四种肝系细胞(肝实质细胞、肝血窦内皮细胞、库否氏细胞及肝星形细胞),两层流道(血窦内腔、窦间隙)共存的体外三维肝血窦模型(图1)。基于该模型,进一步研究发现流动剪切及非实质细胞的共培养均可提高肝细胞的功能;共培养时两种重要的生长因子VEGF和HGF的分泌可能是维持和促进肝细胞功能实现的主要原因。此外,流动剪切和非实质细胞共培养可以增强肝血窦体外模型中肝细胞在细胞色素酶CYP1A2和CYP2D6作用下药物非那西丁和右美沙芬的代谢,在高通量药物筛选方面具有潜在的应用前景。与在体动物实验相比,该模型的条件更加可控且成本较低,具有较高的应用前景。相关工作已作为封面文章在Lab Chip发表,高通量的阵列式筛选平台目前正在进一步优化中。
2)正交流动、三明治肝细胞生物反应器原理样机
目前生物人工肝构建与应用的另一个主要问题是:肝生物反应器器的流动动力学环境设计不够优化,细胞培养的密度与规模化不理想、肝细胞与血浆的物质交换性能不高,不能为肝细胞提供理想的微环境,氧合作用不佳、肝细胞代谢产物无法排除、营养液的物质输运不理想、无免疫阻隔、操作难等。
采用理论分析、数值模拟并结合生物学验证的策略,我们自主研发了正交流动、三明治肝细胞生物反应器原理性样机,其包括培养桶、上盖、下盖及若干个培养单元;上盖和下盖的结构相同,均包括培养液进口、培养液出口;每个培养单元从下至上包括培养液导流片、肝细胞培养片,肝细胞培养片包括圆片框和半透膜,半透膜粘接在圆片框上,在圆片框的圆周上分布多个第一通液孔;培养液导流片是外径等于圆片框外径的圆环形状,在其圆周的两个相对侧上分别具有一个向内径向突起的凸片,在两个凸片的至少一个的圆周处设有多个与第一通液孔对应的第二通液孔;在最上端的培养单元上放置一个培养液导流片。该反应器的半透膜粘接在圆片框上,肝细胞培养液进入半透膜,肝细胞培养片之间通过培养液导流片密封,并且血液与肝细胞培养液有各自的通道,在每个培养单元交替灌液,实现双流路,因此细胞培养的密度与规模化理想、肝细胞与血浆的物质交换性能高,能够为肝细胞提供理想的微环境,氧合作用好、肝细胞代谢产物可以排除、营养液的物质输运理想、具有免疫阻隔、操作简单。目前已经完成原理样机制备和物理验证,正在进行进一步优化中。
应用领域
1)体外三维肝血窦模型:应用于肝脏纤维化/硬化和肿瘤转移的免疫调控机制;相关肝脏疾病的药物筛选;
2)正交流动、三明治肝细胞生物反应器:生物人工肝临床应用。
技术成熟度
目前均已完成原理样机制备及物理验证。